A Pfizer - Comirnaty oltás mellékhatásai - az amerikai Pfizer vakcina várható mellékhatásai
A gyógyszer hivatalos neve:
Comirnaty koncentrátum diszperziós injekcióhoz COVID-19 mRNS vakcina (nukleozid-módosított)
Terápiás javallatok
A Comirnaty aktív immunizálásra javallott a SARS-CoV-2 vírus által okozott COVID-19-betegség megelőzésére, 16 éves és idősebb személyek körében.
Adagolás és alkalmazás
Adagolás 16 évesek és idősebbek: A Comirnaty-t intramuscularisan kell beadni hígítás után, 2 (egyenként 0,3 ml-es) adagból álló sorozatban. A második adag beadása 3 héttel az első után javasolt (lásd 4.4 és 5.1 pont). Nincs adat arra vonatkozóan, hogy a Comirnaty felcserélhető-e más COVID-19-vakcinákkal a vakcinasorozat befejezéséhez. Azoknak, akik már kaptak 1 adag Comirnaty-t, egy második adag Comirnaty-t kell kapniuk a vakcinasorozat befejezéséhez.
Gyermekek és serdülők: A Comirnaty biztonságosságát és hatásosságát 16 évnél fiatalabb gyermekek és serdülők esetében nem igazolták. Korlátozott mennyiségű adat áll rendelkezésre.
Idősek: Dózismódosításra nincs szükség ≥ 65 éves korú, idős személyeknél.
Nemkívánatos hatások, mellékhatások
A biztonságossági profil összegzése
A Comirnaty biztonságosságát 16 éves és idősebb személyek részvételével 2 klinikai vizsgálatban értékelték. Az ezekben közreműködő 21 744 fő legalább egy dózist megkapott a Comirnaty-ból.
A 2. vizsgálatban (Study 2) összesen 21 720 fő –16 éves és idősebb résztvevő – kapott legalább 1 adag Comirnaty-t, és összesen 21 728 fő – 16 éves és idősebb résztvevő – kapott placebót (köztük 16 és 17 éves korú serdülők is, a vakcinát kapó csoportban 138 fő, a placebót kapó csoportban pedig 145 fő). Összesen 20 519 16 éves és idősebb résztvevő kapott 2 dózis Comirnaty-t.
A 2. vizsgálat (Study 2) elemzésének idején összesen 19 067 fő 16 éves és idősebb résztvevőt (9531 fő a Comirnaty-csoportban és 9536 fő a placebocsoportban) értékeltek a biztonságosság szempontjából a Comirnaty második adagjának beadása után legalább 2 hónappal. Ez összesen 10 727 fő (5350 fő a Comirnaty-csoportban és 5377 fő a placebocsoportban), 16–55 éves résztvevőt, és összesen 8340 (4181 fő a Comirnaty-csoportban és 4159 fő a placebocsoportban) 56 éves és idősebb résztvevőt jelent.
A 16 éves és idősebb résztvevők körében leggyakrabban előforduló mellékhatások a következők voltak: fájdalom a beadás helyén (> 80%), kimerültség (> 60%), fejfájás (> 50%), izomfájdalom és hidegrázás (> 30%), ízületi fájdalom (> 20%), valamint láz és az injekció beadási helyén jelentkező duzzanat (> 10%), és ezek általában enyhék vagy közepesen súlyosak voltak, és a vakcina beadása után pár napon belül elmúltak. A magasabb életkorral a reaktogenitási események előfordulási gyakorisága némileg csökken.
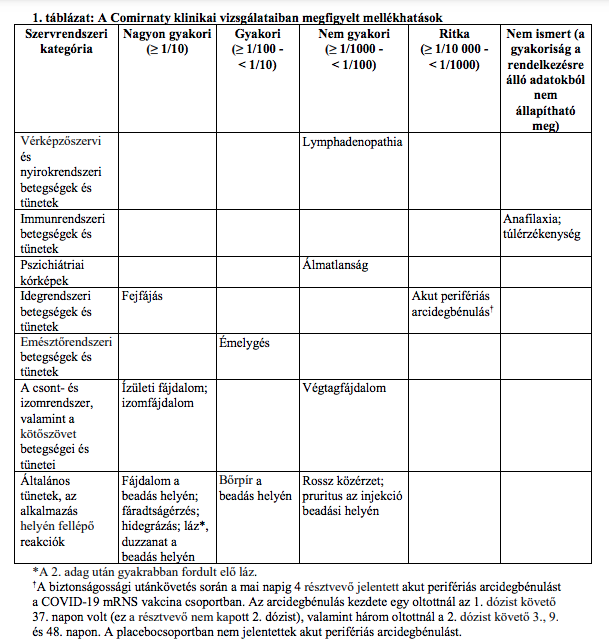
Klinikai vizsgálatokban megfigyelt mellékhatások táblázatos felsorolása
A klinikai vizsgálatok során megfigyelt mellékhatások felsorolása alább található a következő gyakorisági kategóriák szerint:
Nagyon gyakori (≥ 1/10),
Gyakori (≥ 1/100 - < 1/10),
Nem gyakori (≥ 1/1000 - < 1/100),
Ritka (≥ 1/10 000 - < 1/1000),
Nagyon ritka (< 1/10 000),
Nem ismert (a gyakoriság a rendelkezésre álló adatokból nem állapítható meg)
forrás: https://www.ema.europa.eu/en/documents/product-information/comirnaty-epar-product-information_hu.pdf
Az orosz Szputnyik vakcina mellékhatásai.
A kínai Sinopharm vakcina mellékhatásai